แบบ จำลอง ของ อะตอม
วิวัฒนาการของแบบจำลองอะตอมตามลำดับไทม์ไลน์ น้องๆ ม. 4 ที่กำลังเรียนโครงสร้างอะตอมอยู่ หรือพี่ๆที่ต้องการสรุป สามารถนำไปอ่านเพื่อทำความเข้าใจได้นะครับ 🌑 😁 ❗️ ระวัง ❗️ แบบจำลองอะตอมของทอมสันที่มักเข้าใจผิด ❎ ผิด: แบบจำลองอะตอมของทอมสันประกอบไปด้วยประจุบวกและประจุลบในจำนวนที่เท่ากันทำให้อะตอมเป็นกลางทางไฟฟ้า ✅ ถูก: แบบจำลองอะตอมของทอมสันประกอบไปด้วยเนื้ออะตอมที่เป็นประจุบวก และมีอิเล็กตรอนที่เป็นประจุลบกระจายอยู่ทั่วไป โดยประจุบวกและประจุมีขนาดของประจุเท่ากันทำให้อะตอมเป็นกลางทางไฟฟ้า กราฟฟิควิชาเคมีสำหรับนักเรียน ม. ปลาย และเพื่อนครูที่สนใจนำไปประกอบการสอน ฟรี! View more posts เมนูนำทาง เรื่อง
- ประวัติ ของ จำลอง ศรีเมือง
- แบบจําลองของอะตอม
- แบบจำลองอะตอมของรัทเทอร์ ฟอร์ด - แบบจำลองอะตอม
- เนื้อหาเกี่ยวกับโครงสร้างอะตอม - บทเรียนออนไลน์ เรื่อง อะตอม
- แบบจำลองอะตอม | kanokwantaew
ประวัติ ของ จำลอง ศรีเมือง
อิเล็กตรอนไม่ได้เคลื่อนที่เป็นวงกลม แต่เคลื่อนที่ไปรอบๆนิวเคลียส เป็นรูปทรงต่างๆตามระดับพลังงาน 2. ไม่สามารถบอกตำแหน่งที่แน่นอนของอิเล็กตรอนได้เนื่องจากอิเล็กตรอนมีขนาดเล็กมาก และเคลื่อนที่รวดเร็วตลอดเวลาไปทั่วทั้งอะตอม 3. อะตอมประกอบด้วยกลุ่มหมอกของอิเล็กตรอนรอบนิวเคลียส บริเวณที่มีหมอกทึบแสดงว่ามีโอกาสพบอิเล็กตรอนได้มากกว่าบริเวณที่มีหมอกจาง ดังรูปที่แสดงไว้
6 ล้านอิเล็กตรอนโวลต์ พบว่าเมื่ออนุภาคแอลฟาวิ่งผ่านทองคำเปลวโดยมากจะทะลุไปตรงๆ หรือหักเหน้อยมาก แต่ก็มีบางตัวที่หักเหจากแนวเดิมเป็นมุมใหญ่ๆ ดังรูป ผลการทดลองของรัทเทอร์ฟอร์ดสรุปได้ว่า 1. อนุภาคแอลฟาส่วนใหญ่: ผ่านเป็นเส้นตรง แสดงว่าในอะตอมมีที่ว่าง 2. อนุภาคแอลฟาส่วนน้อย: หักเห ( เลี้ยวเบน) แสดงว่าชนกับโปรตอนที่มีมวลมากอยู่ด้านข้างของอะตอม 3.
แบบจําลองของอะตอม
เมื่ออิเล็กตรอนได้รับพลังงานในปริมาณที่เหมาะสม อิเล็กตรอนจะขึ้นไปอยู่ในระดับพลังงานที่สูงกว่าระดับพลังงานเดิมแต่จะอยู่ในระดับใดขึ้นอยู่กับปริมาณพลังงานที่ได้รับการที่เล็กตามขึ้นไปอยู่ในระดับพลังงานใหม่ทำให้ อะตอมไม่เสถียรอิเล็กตรอนจะกลับมาอยู่ในระดับพลังงานที่ต่ำกว่าซึ่งการเปลี่ยนตำแหน่งของแต่ละระดับพลังงานนี้อิเล็กตรอนจะคายพลังงานออกมาในรูปของคลื่นแม่เหล็กไฟฟ้าด้วยความถี่เฉพาะค่าหนึ่งหรือกล่าวได้ว่าการดูดหรือคายพลังงานของอิเล็กตรอนในอะตอมต้องมีค่าเฉพาะตามทฤษฎีของคลังโดยมีค่าเท่ากับความถี่ของคลื่นแม่เหล็กไฟฟ้านั้นคุณด้วยค่าคงที่ของพลังค์ดังกล่าวมาแล้ว 2. การเปลี่ยนแปลงระดับพลังงานของอิเล็กตรอนไม่จำเป็นต้องเปลี่ยนไประดับพลังงานที่อยู่ติดกันอาจมีการเปลี่ยนข้ามระดับพลังงานได้และจะอยู่ระหว่างระดับพลังงานไม่ได้ 3.
แบบจำลองอะตอมของรัทเทอร์ ฟอร์ด - แบบจำลองอะตอม

เนื้อหาเกี่ยวกับโครงสร้างอะตอม - บทเรียนออนไลน์ เรื่อง อะตอม
อิเล็กตรอนจะเคลื่อนที่รอบนิวเคลียสเป็นชั้นๆตามระดับพลังงาน และแต่ละชั้นจะมีพลังงานเป็นค่าเฉพาะตัว 2. อิเล็กตรอนที่อยู่ใกล้นิวเคลียสมากที่สุดจะเรียกว่าระดับพลังงานต่ำสุดยิ่งอยู่ห่างจากนิวเคลียสมากขึ้น ระดับพลังงานจะยิ่งสูงขึ้น 3. อิเล็กตรอนที่อยู่ใกล้นิวเคลียสมากที่สุดจะเรียกระดับพลังงาน n = 1 ระดับพลังงานถัดไปเรียกระดับพลังงาน n =2, n = 3,... ตามลำดับ หรือเรียกเป็นชั้น K, L, M, N, O, P, Q.... แบบจำลองอะตอมแบบกลุ่มหมอก เป็นแบบจำลองที่นักวิทยาศาสตร์คิดว่าเป็นไปได้มากที่สุดทั้งนี้ได้จากการประมวลผลการทดลองและข้อมูลต่างๆ อะตอมภายหลังจากที่นีลส์โบร์ ได้เสนอแบบจำลองอะตอมขึ้นมา อาจสรุปได้ดังนี้ 1. อิเล็กตรอนไม่สามารถวิ่งรอบนิวเคลียสด้วยรัศมีที่แน่นอน บงครั้งเข้าใกล้บางครั้งออกห่าง จึงไม่สามารถบอกตำแหน่งที่แน่นอนได้ แต่ถ้าบอกได้แต่เพียงที่พบอิเล็กตรอนตำแหน่งต่างๆภายในอะตอมและอิเล็กตรอนที่เคลื่อนที่เร็วมากจนเหมือนกับอิเล็กตรอนอยู่ทั่วไปในอะตอมลักษณะนี้เรียกว่า "กลุ่มหมอก" 2. กลุ่มหมอกองอิเล็กตรอนในระดับพลังงานต่างๆจะมีรูปทรงต่างกันขึ้นอยู่กับจำนวนอิเล็กตรอน และระดับพลังงานอิเล็กตรอน 3. กลุ่มหมอกที่มีอิเล็กตรอนระดับพลังงานต่ำจะอยู่ใกล้นิวเคลียสส่วนอิเล็กตรอนที่มีระดับพลังงานสูงจะอยู่ไกลนิวเคลียส 4.
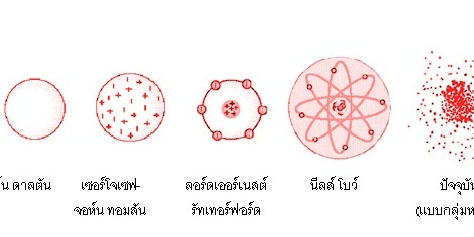
แบบจำลองอะตอมที่เป็นที่รู้จักดีมีอยู่ 5 แบบ คือ 1. แบบจำลองอะตอมของดอนตัลซึ่งมีลักษณะป็นทรงกลมและภายในว่างเปล่าไม่มีอะไรไม่สามารถทำให้สูญหายหรือเกิดขึ้นใหม่ได้ 2. แบบจำลองอะตอมของทอมสันซึ่งภายในอะตอมมีโปรตอนและมีอิเล็กตรอนเท่าๆกันกระจัดกระจายอยู่ทั่วภายในอะตอม 3. แบบจำลองอะตอมของรัทเทอร์ฟอร์ดซึ่งภายในนิวเคลียสของอะตอมมีโปรตอนและนิวตรอนอยู่ภายในส่วนบริเวณนอกมีอิเล็กตรอนวิ่งอยู่รอบๆอย่างอิสระ 4. แบบจำลองอะตอมของโบร์ซึ่งภายในอะตอมจะมีชั้นพลังงานและแบ่งเป็นชั้นได้7ชั้นคือ k l m n o p q ตามลำดับซึ่งแต่ละระดับชั้นพลังงานก็จะมีพลังงานที่ไม่เท่ากัน 5. แบบจำลองอะตอมของกลุ่มหมอก ภายในตรงกลางนิวเคลียสจะเป็นโปรตอนและนิวตรอน ส่วนภายนอกเป็นกลุ่มหมอก ถ้ากลุ่มหมอกตรงบริเวณไหนมากก็แสดงว่าตรงนั้นมีโอกาสที่จะมีอิเล็กตรอนอยู่มากกว่าที่อื่นๆ แบบจำลองอะตอมที่ได้รับการยอมรับมากที่สุดในปัจจุบันคือแบบจำลองอะตอมของกลุ่มหมอก
แบบจำลองอะตอม | kanokwantaew
- เกิดอะไรขึ้นกับ "มังกรฟ้า" หลังถูกบุกตรวจสอบสลากเกิน 80 บาท เตรียมปิดเว็บมังกรฟ้า หยุดขายสลากกินแบ่งรัฐบาลตั้งแต่งวด 16 เม.ย.
- แบบจำลองอะตอมของโบร์ - แบบจำลองอะตอม
- ประวัตินักวิทยาศาสตร์และการค้นพบอะตอม
- Panasonic lumix g95 ราคา firmware
- แบบจำลองอะตอม | kanokwantaew
- เคมี: แบบจำลองอะตอม
- ซี วิ ค 2004
- ซื้อ "ของออนไลน์" จากต่างประเทศ ต้องเตรียมเงินจัดการภาษีเท่าไหร่ ?

303 X 10 -18 J Note: พลังงานที่ได้มีค่าเป็นลบ 0. 303 X 10 -18 J แสดงว่าอิเล็กตรอนคายพลังงาน 0. 303 X 10 -18 J พลังงานที่ปล่อยออกมานี้มีความยาวคลื่น 656. 3 นาโนเมตร ซึ่งเป็นความยาวคลื่นของแสงสีแดง ที่อยู่ในช่วงที่ตามองเห็น เราจึงเห็นเส้นสเปกตรัมสีแดงปรากฎบนฉากรับภาพ คำนวณจาก เมื่อ D E = ความแตกต่างของพลังงานระหว่าง 2 ระดับพลังงาน h = ค่าคงที่ของพลังค์ = 6. 626 X 10 -34 Js c = ความเร็วของคลื่นแม่เหล็กไฟฟ้าในสุญญากาศ = 2. 997 X 10 8 m/s = ความยาวคลื่น หน่วยเป็นเมตร(m) แทนค่า ดังนั้น การเปลี่ยนระดับพลังงานจาก n=3 n=2 เกิดสเปกตรัมสีแดง ส่วน n=4 n=2, n=5 n=2 และ n= n=2 นั้นให้สีของเส้นสเปกตรัมไม่เหมือนกัน ดังตาราง n i (ระดับพลังงานเริ่มต้น) n f (ระดับพลังงานสิ้นสุด) ความยาวคลื่น(นาโนเมตร) เส้นสเปกตรัม 3 2 656. 3 สีแดง 4 2 486. 1 สีน้ำทะเล 5 2 434. 0 สีน้ำเงิน 2 410. 2 สีม่วง แบบจำลองอะตอมของโบร์ หมายเหตุ ภาพแสดงอิเล็กตรอนหมุนรอบนิวเคลียสไม่ได้แสดงความเร็วของอิเล็กตรอนที่แท้จริง อะตอมประกอบด้วยโปรตอนและนิวตรอน อยู่ภายในนิวเคลียส ส่วนอิเล็กตรอนวิ่งอยู่รอบ ๆ นิวเคลียสเป็นชั้น ๆ หรือเป็นระดับพลังงานซึ่งมีค่าเป็นขั้น ๆ อย่างเด็ดขาด ไม่มีค่าที่ต่อเนื่องกัน ประโยชน์ที่เราสามารถนำไปประยุกต์ใช้ได้จากงานของโบร์ 1.